Szeptember közepén Stockholmban tartották az idei ECTRIMS konferenciát, melynek legérdekesebb előadásaiból és posztereiből az alábbiakban szemezgetünk.
Szeptember közepén Stockholmban tartották az idei ECTRIMS konferenciát, melynek legérdekesebb előadásaiból és posztereiből az alábbiakban szemezgetünk.
Címke: ocrelizumab
Az ocrelizumab megérkezett Európába
 Az Európai Bizottság engedélyezte az első ocrelizumab hatóanyagú gyógyszer forgalomba hozatalát az unió 28 tagállamában. Ezzel egyfelől egy igen versenyképes szerrel bővült a relapszáló-remittáló sclerosis multiplex kezelésére alkalmas betegségmódosító terápiák skálája, másfelől végre az elsődleges progresszív sclerosis multiplex betegek részére is fel tud kínálni valamit az orvostudomány. Ez utóbbi SM típus kezelésére ugyanis eddig semmilyen eszköz nem állt rendelkezésükre. Az Európában élő 700 000 SM beteg közül körülbelül 96 000 személy él ezzel a betegségnek ezzel a fajtájával.
Az Európai Bizottság engedélyezte az első ocrelizumab hatóanyagú gyógyszer forgalomba hozatalát az unió 28 tagállamában. Ezzel egyfelől egy igen versenyképes szerrel bővült a relapszáló-remittáló sclerosis multiplex kezelésére alkalmas betegségmódosító terápiák skálája, másfelől végre az elsődleges progresszív sclerosis multiplex betegek részére is fel tud kínálni valamit az orvostudomány. Ez utóbbi SM típus kezelésére ugyanis eddig semmilyen eszköz nem állt rendelkezésükre. Az Európában élő 700 000 SM beteg közül körülbelül 96 000 személy él ezzel a betegségnek ezzel a fajtájával.
Mikortól lesz elérhető Magyarországon?
Egyelőre arról sincs információnk, mikortól lesz elérhető a gyógyszer a gyakorlati életben. A hatóanyagról a kezelőorvosnál érdemes érdeklődni, mert valószínűleg ő fogja tudni a leghamarabb megmondani, hogy mikor lesz a hazai gyakorlatban is ténylegesen elérhető és választható ilyen gyógyszer.
De mi is ez az ocrelizumab?
A gyógyszer legfontosabb ismérveiről itt írtunk:
Mi az ocrelizumab?
A működési mechanizmusáról és a hatásosságáról itt számoltunk be:
Új hatóanyag az SM kezelésére
Az ocrelizumab közelít az európai piac felé
Az FDA márciusban engedélyezte az első ocrelizumab hatóanyagú szer amerikai forgalmazását a sclerosis multiplex relapszáló-remittáló és elsődleges progresszív formájának kezelésére. Akkor még csak bizakodtunk, hogy az amerikainál szigorúbb európai hivatal is utat enged a gyógyszernek az Európai Unió betegei felé.
Két nappal ezelőtt azonban az EMA emberi felhasználásra szánt gyógyszereket elbíráló bizottsága (CHMP) is javasolta a gyógyszer forgalomba hozatali engedélyének megadását az EU-ban. A CHMP továbbítja ajánlását az Európai Bizottságnak, ami a gyógyszerek engedélyezéséért felel az EU-ban.
 Az Európai Bizottság rendszerint 2-3 hónappal a hivatalos ajánlást követően dönt a forgalomba hozatal engedélyezéséről. A forgalmazási engedély kiadása után a gyógyszer árazásáról az EU tagállamai már külön-külön állapodnak meg, figyelembe véve a gyógyszer potenciális szerepét az adott ország egészségügyi rendszerén belül.
Az Európai Bizottság rendszerint 2-3 hónappal a hivatalos ajánlást követően dönt a forgalomba hozatal engedélyezéséről. A forgalmazási engedély kiadása után a gyógyszer árazásáról az EU tagállamai már külön-külön állapodnak meg, figyelembe véve a gyógyszer potenciális szerepét az adott ország egészségügyi rendszerén belül.
A hatóanyag hazai színre lépésével egyfelől bővülni fog az RRSM kezelésére alkalmas betegségmódosító terápiák skálája, másfelől ez lesz az első PPSM-re is felkínálható szer. A PPSM kezelésére ugyanis jelenleg még semmilyen eszköz nincs az orvosok kezében.
Az ocrelizumab működési mechanizmusáról és hatásosságáról itt írtunk.
Bővebben:
New medicine for multiple sclerosis
Az idei ECTRIMS konferencia hírei a gyógyszerekről
Másfél hete Párizsban tartották az ECTRIMS konferenciát, ahol különböző kutatási eredményeket osztottak meg egymással a szakma képviselői. A konferencia anyagának sclerosis multiplex gyógyszerekkel kapcsolatos részeiből szemezgettünk.
Új hatóanyag a sclerosis multiplex kezelésére: piacra került az ocrelizumab
A tegnapi napon az FDA engedélyezte az első ocrelizumab hatóanyagú gygóyszer amerikai forgalmazását a sclerosis multiplex relapszáló-remittáló és elsődleges progresszív formájának kezelésére. Ez a lépés elsősorban a progresszív betegek számára bír életbevágó jelentőséggel, hiszen az orvostudománynak eddig semmilyen eszköze nem volt az ő betegségük megfékezésére. Ugyanakkor a relapszáló pácienseknek is minden okuk megvan az örömre, hiszen a kísérletek szerint az ocrelizumab az esetek közel felében teljesen megállította az RRSM lefolyását.
Hogyan működik az ocrelizumab?
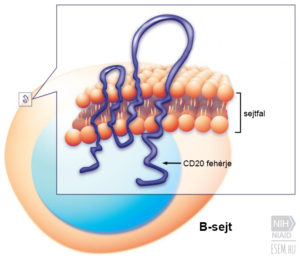
A legtöbb SM-gyógyszer a T-sejtekre fejti ki hatását. Ezzel szemben az ocrelizumab a B-sejteket veszi célba. A B-sejtek felületén ugyanis van egy CD20-nak keresztelt fehérjemolekula, aminek nagyobb szerepe van a betegség lefolyásában, mint azt korábban gondolták. A CD20-as B-sejtek közvetlen kárt okoznak a myelinhüvelyben és magában az idegsejtben egyaránt. Az ocrelizumab a CD20 molekula ellenanyaga, ami az érett B-sejteket megtámadva fejti ki hatását.
Mindez persze nem érvényteleníti a T-sejtek érintettségét SM-ben. A B-sejtek a T-sejtekkel karöltve felelősek a gyulladásos agyi léziókért és ennélfogva a betegek állapotának súlyosbodásáért. Az ocrelizumab működési elve azért rendhagyó, mert az eddigi terápiák a T-sejteken keresztül fejtették ki hatásukat. Ezt úgy lehet elképzelni, mint két utat, amelyek egy idő után egybefutnak. Eddig mindenki a T-utat taposta, de most végre valaki a B-útvonalat is felfedezte. Igaz, hogy a végén a két szál összefut, de azzal, hogy a B-úton vívott harc erőteljesebb, az ocrelizumab az SM minden eddiginél hatékonyabb kezelési módja lett.
Mennyire hatásos az ocrelizumab?
2011-ben sokakat meglepett, hogy a B-sejteket célba véve a betegek kétharmada tünetmentessé vált: sem új léziójuk nem keletkezett, sem új relapszuson nem estek át, és a progressziónak semmi jelét nem mutatták.
A gyógyszer hatásfoka azonban a további kísérletek során vált egyre világosabbá.
Egy több mint két éven keresztül folytatott, elsődleges progresszív betegek körében végzett vizsgálat során fél év alatt 25%-kal sikerült csökkenteni a progresszió mértékét a placebóhoz képest, valamint a páciensek 42%-a semmiféle progressziót nem mutatott a bő két év során.
(A tanulmány fedőneve az ORATORIO volt.)
A relapszáló betegek körében végzett két vizsgálatban kontrollként nem placebót, hanem egy interferon-béta-1a hatóanyagú gyógyszert alkalmazták, és annak hatásfokához viszonyították az ocrelizumab eredményeit. A másik szerhez képest az új gyógyszer 46 illetve 47%-kal csökkentette az éves relapszus-számot, 94 illetve 95%-kal csökkentette az új léziók számát közel két év alatt, és a betegek 64 illetve 89%-a maradt teljesen tünetmentes (a tünetmentességbe beleszámították az agyi léziókat, a tüneteket okozó relapszusokat és a progressziót egyaránt). Ráadásul minél tovább kezelték a betegeket az ocrelizumabbal, annál többük érte el a teljes tünetmentességet.
(A tanulmányok fedőnevei az OPERA I és OPERA II voltak.)
Mik az ocrelizumab mellékhatásai?
Minden gyógyszernek, ami hat a szervezetre, mellékhatásai is vannak. Ez alól sajnos az ocrelizumab sem kivétel. Ugyanakkor a terápiás hatás mértékéhez képest az ocrelizumab meglepően kíméletes a szervezetre.
Az ocrelizumabbal és a placebóval kezelt elsődleges progresszív betegek között, valamint az ocrelizumabbal és az interferon-béta-1a-val kezelt relapszáló betegek között egyaránt azonos mértékű mellékhatásokat tapasztaltak, az enyhe és a súlyos mellékhatásokat is beleértve.
Minden immunrenszerre ható gyógyszer esetében jogos aggodalom a fertőzésekre való hajlam, de az ocrelizumab szerencsére ebben sem igazán különbözött a két-két kísérleti csoport között. Csupán néhány olyan enyhe fertőzés volt gyakoribb az ocrelizumabbal kezelt relapszáló betegek között, mint a megfázás és a herpesz. Ez a kíméletes hatásmechanizmus annak köszönhető, hogy az ocrelizumab nem az őssejteket vagy a plazmasejteket veszi célba, amelyek az antitestek termelését végzik. A CD20 molekula nincs jelen minden immunsejten, csak egy kis hányadukon, így a többiek zavartalanul fel tudják venni a harcot a fertőzésekkel és egyéb megbetegedésekkel szemben.
A rossz hír azonban, hogy mindhárom vizsgálat során az derült ki, az ocrelizumab megduplázza a rák kialakulásának esélyét.
Mikor lesz elérhető Magyarországon is?
 Az FDA tegnapi engedélyezése csak az Egyesült Államokban történő használatra érvényes. Noha ott már két héten belül az orvosi protokoll részévé válik a gyógyszer használata, az európai piac kapui még zárva vannak az ocrelizumab előtt. Az engedélyezési kérelem már be lett adva az EMA felé is, akik minden valószínűség szerint az FDA-hoz hasonló pozitív ítéletet fognak hozni, így remélhetőleg hamarosan az Európai Unió országaiban élő betegek számára is elérhetővé válik ez az új terápiás lehetőség.
Az FDA tegnapi engedélyezése csak az Egyesült Államokban történő használatra érvényes. Noha ott már két héten belül az orvosi protokoll részévé válik a gyógyszer használata, az európai piac kapui még zárva vannak az ocrelizumab előtt. Az engedélyezési kérelem már be lett adva az EMA felé is, akik minden valószínűség szerint az FDA-hoz hasonló pozitív ítéletet fognak hozni, így remélhetőleg hamarosan az Európai Unió országaiban élő betegek számára is elérhetővé válik ez az új terápiás lehetőség.
Forrásként szolgáló cikkek
FDA Approves Ocrelizumab as 1st MS Treatment for Both Relapsing and Primary Progressive Forms
A Journey from Defiant Idea to Game-Changing Treatment
5 Things to Know About the New MS Drug
The Hope of ‘Ending MS Forever’: Interview with MS Society’s Tim Coetzee
Az idei ACTRIMS konferencia hírei
Hamarosan itt az első gyógyszer progresszív SM-re
Amerikai neurológusok ez év végére várják, hogy az FDA engedélyezze az első ocrelizumab hatóanyagú gyógyszert. Ez lesz az első olyan szer, ami a relapszáló-remittáló SM mellett a progresszív SM-re is pozitív hatással van, ezért nagy várakozás övezi az engedélyeztetést. A megkérdezett neurológusok harmada már tervbe vette a szer felírását betegeinek.
 A gyógyszer hatásmechanizmusa eltér az eddig használt szerektől, mert az nem az immunrendszer T-sejtjeit, hanem a CD20-pozitív B-sejtjeit veszi célba. A feltételezések szerint ez utóbbiak indítják el azokat a folyamatokat, amik végül a rokkantsághoz vezetnek.
A gyógyszer hatásmechanizmusa eltér az eddig használt szerektől, mert az nem az immunrendszer T-sejtjeit, hanem a CD20-pozitív B-sejtjeit veszi célba. A feltételezések szerint ez utóbbiak indítják el azokat a folyamatokat, amik végül a rokkantsághoz vezetnek.
A placebót szedő elsődleges progresszív SM betegekhez képest a hatóanyaggal kezelt páciensek csoportjában 47%-kal nőtt azok száma, akiknél nem volt kimutatható betegségrosszabbodás a 2 és fél éven át tartó kísérlet utolsó 3 hónapjában. Relapszáló SM-esek (RRSM és SPSM relapszusokkal) esetén az interferon-béta-1a-hoz hasonlítva ez az érték 75%-ra jött ki egy 2 évig tartó kísérlet során.
Bővebben:
Neurologists Anticipate FDA Approval of the 1st Progressive MS Treatment
Phase III efficacy results of investigational medicine ocrelizumab reinforced by exploratory analyses in two forms of multiple sclerosis