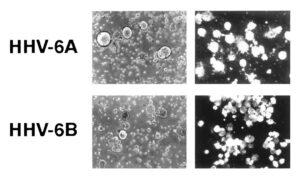
Egy több mint 15 000 személy bevonásával végzett svéd kutatás szerint a herpeszvírus 6A (azaz a HHV-6A), és nem a széles körben elterjedt 6B (azaz a HHV-6B) típusa lehet a sclerosis multiplex egyik kiváltó oka.
Az elterjedtebb 6B típus olyan gyakori, hogy becslések szerint a gyerekek kb. 80%-a két éves kora előtt megfertőződik vele. Ez olyan, viszonylag enyhe lefolyású betegségeket okoz, mint például a háromnapos láz (más néven roseola). Ehhez a vírushoz annyira hasonlít a nála sokkal ritkábban előforduló 6A típus, hogy az orvostudomány mindeddig nem is tudott különbséget tenni kettejük között. Ezúttal úgy tudták elkülöníteni a két típust egymástól, hogy azokat a herpesz vírus ellen termelt antitesteket vetették össze egymással a vérben, amelyek azokat a fehérjéket ismerik fel, amelyek leginkább eltérnek a két herpeszvírus között.
Az SM betegek vérében több HHV-6A vírus elleni antitest van, mint az egészséges emberek szervezetében. A HHV-6A vírus okozta fertőzés több mint kétszeresére növeli az SM későbbi kialakulásának kockázatát. A jelek szerint minél fiatalabb korban fertőződik meg valaki, annál nagyobb eséllyel válik SM beteggé az élete során. Ezzel szemben a HHV-6B elleni antitestek nem mutattak összefüggést az SM kialakulásával, sőt, az SM betegek kevesebb HHV-6B elleni antitestet termeltek, mint az egészséges személyek.
Bővebben:
Gyakori herpeszvírusokhoz köthető a sclerosis multiplex kialakulása → Arsratio
MS Risk Linked to Herpes Virus 6A and Not More Common 6B, Study Suggests → MS News Today